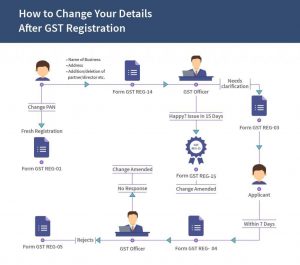
Bagaimana rumus menentukan pH asam dan basa?
Bagaimana rumus menentukan pH asam dan basa?
- Rumus Asam dan Basa Kuat.
- [H+] = Ma . valensi asam.
- [OH-] = Mb . valensi basa.
- Valensi adalah jumlah ion H+ atau OH- dalam reaksi.
- pH = – log [H+]
- pOH = -log [OH-]
- pH = pKw – pOH = 14 – pOH.
- Rumus Asam dan Basa Lemah.
Bagaimana rumus menghitung pH?
Persamaan pH dapat dilihat sebagai berikut: pH = -log[H3O+].
- Persamaan terkadang dapat dilihat sebagai pH = -log[H+].
- Tidaklah penting untuk mengetahui arti log negatif agar dapat menghitung pH. Kebanyakan kalkulator yang digunakan di sekolah menengah dan universitas memiliki tombol log.
Berapa pH larutan asam basa?
Air murni bersifat netral, dengan pH-nya pada suhu 25 °C ditetapkan sebagai 7,0. Larutan dengan pH kurang daripada tujuh disebut bersifat asam, dan larutan dengan pH lebih daripada tujuh dikatakan bersifat basa atau alkali.
Berapa satuan pH?
PH adalah tingkat keasaman atau kebasaan yang diukur dengan menggunakan skala pH antara 0 sampai 14.
Berapa nilai pH larutan?
Berapa pH dari 0 1 M HCl?
Jawab : pH dari larutan HCl 0,01 M adalah 2.
Apa yang dimaksud dengan asam kuat dan asam lemah?
Asam kuat adalah senyawa yang terurai secara keseluruhan saat di larutkan di dalam air dan menghasilkan jumlah ion seluruhnya. Basa kuat adalah senyawa yang terurai secara keseluruhan saat dilarutkan ke dalam air. Asam lemah adalah senyawa yang sedikit terurai saat dilarutkan di dalam air.
Larutan penyangga apa saja?
Secara umum, larutan penyangga terbagi menjadi dua jenis, yaitu:
- Larutan Penyangga Asam.
- Larutan Penyangga Basa.
- Rumus Larutan Penyangga Asam.
- Rumus Larutan Penyangga Basa.
- Air Ludah Sebagai Larutan Penyangga.
- Darah sebagai Larutan Penyangga.
- Menjaga Keseimbangan pH Tanaman.
Berapa rentangan pH asam dan basa?
Indikator universal
| Rentang pH | Keterangan | Warna |
|---|---|---|
| 3-6 | Asam lemah | Jingga/Kuning |
| 7 | Netral | Hijau |
| 8-11 | Basa lemah | Biru |
| > 11 | Basa kuat | Ungu/violet |
Apa saja sifat asam?
Secara umum, asam memiliki sifat sebagai berikut:
- Rasa: masam ketika dilarutkan dalam air.
- Sentuhan: asam terasa menyengat bila disentuh, dan dapat merusak kulit, terutama bila asamnya asam pekat.
- Kereaktifan: asam bereaksi hebat dengan kebanyakan logam, yaitu korosif terhadap logam.
Apakah yang dimaksud dengan nilai pH?
PH adalah derajat keasaman atau kebasaan suatu larutan, menyatakan logaritma negative konsentrasi ion H dengan bilangan pokok 10. Larutan netral mempunyai PH 7, asam lebih kecil dari 7, basa lebih besar dari 7.Di perairan yang tidak tercemar PH di control oleh ion CO2, Carbonate dan Bicarbonate.
Apa yang dimaksud dengan pH?
pH merupakan indikator tingkat asam atau basa pada air yang dinilai dengan skala 0-14. Air yang netral alias tidak basa maupun asam memiliki kandungan pH sebesar 7. Air asam memiliki pH kurang dari 7 dan air basa lebih dari 7. Setiap angka ini menggambarkan perubahan derajat asam/basa sebesar 10-kali lipat.
Bagaimana untuk menghitung nilai pH dari asam kuat?
Untuk menghitung nilai pH dan pOH dari basa kuat dapat dihitung dengan rumus berikut : 1. Hitunglah pH dan pOH dari 10 liter larutan H2SO4 0,02 M! 2. Hitunglah pH dan pOH dari 1 liter larutan Ca (OH) 2 0,05 M! 3. Jika diketahui suatu asam kuat memiliki konsentrasi H+ sebesar 10-10 M, maka tentukan nilai pH larutan tersebut!
Bagaimana untuk menunjukkan perubahan pH larutan asam basa?
Jika suatu pH larutan asam basa telah diplotkan sebagai fungsi dari volum larutan basa atau asam tersebut yang sudah diteteskan, maka akan diperoleh suatu grafik yang bisa disebut kurva titrasi. Kurva titrasi dapat menunjukkan suatu perubahan pH larutan selama proses titrasi asam dengan basa berlangsung atau sebaliknya.
Bagaimana untuk menghitung larutan asam?
Untuk menghitung suatu larutan asam, maka kita harus mengetahui terlebih dahulu larutan asam tersebut termasuk asam kuat atau asam lemah sebab rumusnya berbeda. Berdasarkan banyak sedikitnya H+ yang dilepaskan, larutan asam dapat dibagi menjadi 2 yaitu asam kuat dan asam lemah. [H+] = x . Ma Hitunglah pH larutan 100 mL H2SO4 0,1 M ! [H+] = x . Ma
Apakah asam kuat dan lemah?
Asam terbagi atas 2, yaitu asam kuat dan lemah. Dalam perhitungannya relatif mudah dan rumusnya pun berbeda. Di bawah ini adalah ciri-ciri asam kuat: Mengion sempurna (derajat ionisasi atau α bernilai 1) pH-nya ditentukan dari konsentrasi larutan dan valensi asam (tentang valensi asam, klik)